 En las últimas décadas, el predominio de la enfermedad del hígado graso no alcohólico (EHGNA) ha ido aumentando exponencialmente y se espera que continúe en aumento. Se cree que la EHGNA puede provocar cirrosis, insuficiencia hepática y carcinoma hepatocelular (CHC). En EE. UU. se ha convertido en una de las principales indicaciones de trasplante hepático.
En las últimas décadas, el predominio de la enfermedad del hígado graso no alcohólico (EHGNA) ha ido aumentando exponencialmente y se espera que continúe en aumento. Se cree que la EHGNA puede provocar cirrosis, insuficiencia hepática y carcinoma hepatocelular (CHC). En EE. UU. se ha convertido en una de las principales indicaciones de trasplante hepático.
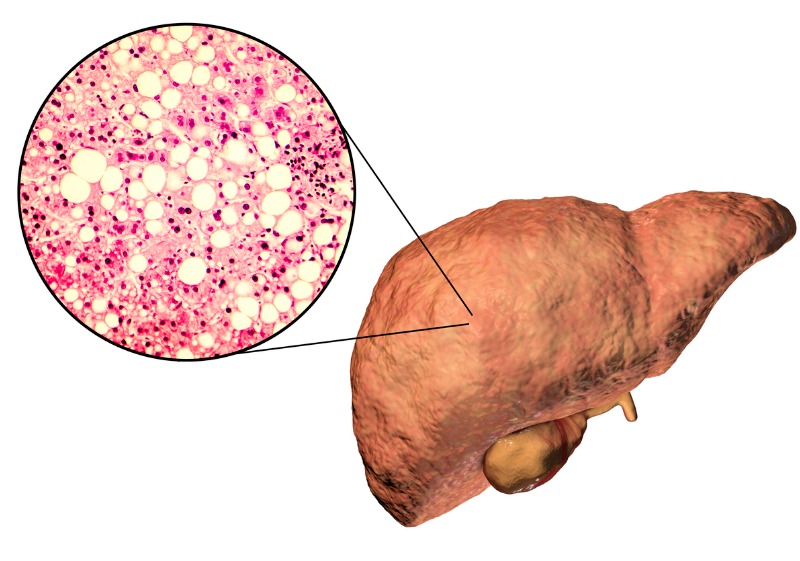
Se define como la acumulación de esteatosis en ≥5% de los hepatocitos, en ausencia de consumo excesivo de alcohol (<20 g/día para las mujeres y <30 g/día para los hombres).
Abarca un amplio espectro de enfermedades hepáticas, que oscila entre dos tipos histológicos diferentes: el hígado graso no alcohólico, una enfermedad relativamente benigna y la esteatohepatitis no alcohólica (EHNA), un proceso más grave.
El hígado graso no alcohólico se define por la presencia de esteatosis hepática sin evidencia de lesión hepatocelular, mientras que la esteatohepatitis no alcohólica (EHNA) lo hace por la presencia de esteatosis acompañada de inflamación lobulillar, balonización (muerte celular) de los hepatocitos, con o sin fibrosis).
El hígado graso no alcohólico tiene un riesgo bajo de complicaciones relacionadas con el hígado, considerando que la EAHA tiene un curso potencialmente progresivo que puede conducir a la fibrosis hepática, cirrosis, hepatopatía en etapa terminal, CHC y/o trasplante hepático, así como complicaciones extrahepáticas, especialmente enfermedades cardiovasculares (ECV), malignidad extrahepática y enfermedad renal crónica. En la actualidad, hasta el 30% de los estadounidenses con EHGNA tienen EHNA, y en hasta el 20% de ellos han desarrollado o desarrollarán fibrosis avanzada a partir de la EHNA.
Una vez que los pacientes desarrollan fibrosis hepática avanzada, el riesgo de morbilidad relacionada con el hígado y la mortalidad aumentan considerablemente. Por lo tanto, el desafío para los médicos de atención primaria (MAP) es identificar tempranamente a los pacientes con un riesgo elevado de EHGNA con fibrosis avanzada que necesitarán ser remitidos al hepatólogo para seguimiento y tratamiento de complicaciones hepáticas, la planificación terapéutica posible y, en caso de enfermedad hepática en etapa terminal, la evaluación para la indicación de un trasplante. Sin embargo, es frecuente que la EHGNA sea infradiagnosticada. A menudo, cuando los pacientes llegan a las clínicas especializadas, se encuentran en una etapa avanzada de la enfermedad, cuando las opciones terapéuticas son limitadas.
En un estudio reciente, en 2 de cada 3 pacientes con EHGNA y cirrosis, esta última fue diagnosticada incidentalmente. Por otra parte, en una encuesta realizada a médicos de atención primaria (MAP), el 85% subestimó la prevalencia de la EHANA mientras que el 78% no se consideraron bien preparados para manejar a los pacientes con EHGNA/EHNA. La paradoja de la EHGNA como enfermedad de gran prevalencia, entre la que solo una pequeña proporción progresa hasta la gravedad, ha llevado a que, en la actualidad, la EHGNA sea considerada de los problemas de salud pública más desafiantes en todo el mundo. Se requieren políticas que abarquen a toda la población para identificar, derivar y manejar a esos pacientes.
Una estrategia exitosa incluiría herramientas sencillas y rentables, y algoritmos, para que los MAP evalúen, diagnostiquen y deriven a los hepatólogos a los pacientes con riesgo elevado de desarrollar complicaciones hepáticas para un mayor estudio y manejo, Así, los pacientes con bajo riesgo de desarrollar esas complicaciones podrían ser manejados por los MAP.
La estratificación eficaz del riesgo aumentaría la derivación de pacientes de riesgo elevado y disminuiría la derivación de aquellos con bajo riesgo, es decir, mejoraría el acceso a la atención médica y la asignación de recursos a los que más lo necesitan.
| Factores de riesgo comunes para la EHGNA |
La enfermedad del hígado graso no alcohólico (EHGNA) está estrechamente asociada a la resistencia a la insulina y suele ser considerada la manifestación hepática del síndrome metabólico.
En un metanálisis de 2016 sobre pacientes con EHGNA, las tasas de obesidad, diabetes mellitus tipo 2 (DMT2), dislipidemia e hipertensión fueron 51%, 23%, 69% y 39%, respectivamente. La DMT2 es uno de los factores de riesgo más fuertes para el desarrollo de EHGNA, fibrosis avanzada/cirrosis, CHC y mortalidad.
Por otra parte, la asociación subyacente de EHGNA y DMT2 es bidireccional, lo que sugiere que la EHGNA puede preceder y/o facilitar el desarrollo de DMT2 y promover resultados adversos asociados con la diabetes. Se estima que entre el 40% y el 70% de los pacientes con DMT2 tienen EHGNA, y que entre ellos, el 37% tiene EHNA y el 17% desarrollará fibrosis.
Por extrapolación, se calcula que entre los diabéticos tipo 2 de EE. UU. la mayoría tienen EHGNA (casi 2 veces y media más que los que presentan EHNA). Le siguen en número los que están en menor riesgo de fibrosis avanzada. De manera similar a la DMT2, la obesidad es prevalente en la población general. En EE. UU., según una encuesta nacional, el 42,9% de los adultos son actualmente obesos y el 9,2% son extremadamente obesos (definidos por un índice de masa corporal ≥40 kg/m2).
La obesidad es uno de los factores de riesgo más importantes para la EHGNA y se ha relacionado con la presencia y gravedad de la fibrosis hepática.
Un estudio prospectivo de cohorte, de 40.700 pacientes con EHGNA, mostró que la obesidad y el aumento de peso fueron predictores independientes de la presencia de fibrosis hepática. También se han hallado determinantes genéticos y epigenéticos que representan un papel en la historia natural de los pacientes con EHGNA, particularmente porque en los familiares de los pacientes con EHNA, la enfermedad es más grave.
Estudios de asociación del genoma completo han revelado vínculos entre polimorfismos de nucleótidos individuales específicos y el curso de la enfermedad, incluyendo el contenido de los genes PNPLA3 (patatin-like phospholipase domain-containing 3 (PNPLA3), TM6SF2 (transmembrane 6 superfamily member 2) y, más recientemente, HSD17B13 (17-ß hidroxiesteroide deshidrogenasa 13), MBOAT7 (membrane-bound O-acyltransferase domain-containing 7, y las variantes TMC4 (transmembrane channel-like 4).
Vea el texto completo en:



