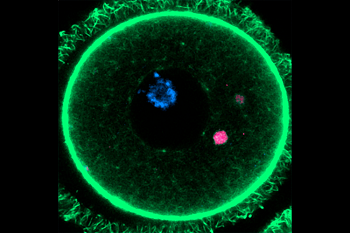
Un equipo del grupo de la doctora Elvan Böke, del Centro de Regulación Genómica (CRG) de Barcelona, ha descubierto un nuevo mecanismo que explica cómo los óvulos inmaduros –ovocitos– permanecen en perfectas condiciones durante décadas, lo que podría permitir explorar las causas de la infertilidad.
La existencia de generaciones futuras depende de que la reserva finita de óvulos inmaduros (ovocitos) sobreviva durante muchos años sin sufrir daños. Cómo logran esta hazaña de longevidad, de hasta casi medio siglo en el caso de los seres humanos, ha sido un misterio poco estudiado hasta ahora.
Para resolverlo, el estudio, publicado esta semana en la revista Cell, se centra en los agregados de proteínas, que son grupos de proteínas mal plegadas o dañadas. Si no se controlan, estas sustancias nocivas se acumulan y tienen efectos altamente tóxicos.
Se sabe que los agregados de proteínas se acumulan en las neuronas y sus efectos se han relacionado con enfermedades neurodegenerativas como el Alzheimer. La mayoría de las células manejan los agregados descomponiéndolos, pero la larga vida de los ovocitos hace que esa estrategia no sea viable y provoca que sean muy sensibles a las proteínas dañadas.
En un encuentro organizado por SMC España, el investigador del CRG y coautor del estudio, Gabriele Zaffagnini, ha recordado que la fertilidad femenina decrece con la edad. «O sea, cuanto más envejece una mujer, menos fértil es. Y esto se debe principalmente a una reducción en la calidad de sus óvulos», ha afirmado.
Una mujer nace ya con toda la reserva de óvulos que utilizará durante toda su vida fértil. Sin embargo, con el paso del tiempo, esta reserva se va extinguiendo poco a poco, hasta que prácticamente se acaba con la menopausia.
«El óvulo, que es una célula superlongeva, vive décadas, pero tiene que mantenerse limpia e intacta para poder pasar todos sus componentes, además del ADN, al nuevo organismo», ha explicado Zaffagnini, en declaraciones a los medios.
«Entonces, lo que nos ha interesado estudiar era cómo los óvulos se defienden de la agregación de proteínas. Las neuronas y otras células son muy sensibles a la agregación de proteínas. Pero, ¿cómo hacen los óvulos para defenderse de ello?», se ha preguntado, señalando que se puede aprender «algo nuevo» estudiando los óvulos.
Desaparecen cuando el óvulo es fertilizado
Cuando el espermatozoide fertiliza este óvulo y se da lugar a un embrión, los agregados de proteínas poco a poco van desapareciendo. Esto ocurre porque, si el embrión hereda agregados, no se desarrolla.
Para este proceso de “destrucción”, los óvulos “secuestran” a estos tóxicos en compartimentos especiales, denominados conjuntos vesiculares endolisosomales (ELVAs). «Estos compartimentos se componen de lisosomas, que son los orgánulos que se encargan de degradar la basura», ha desgranado el coautor de la investigación.
Según el autor, los ELVAs permanecen inactivos en óvulos inmaduros y se activan para destruir los agregados cuando maduran; o sea, cuando se prepara para ser fertilizado.
«Lo que hemos encontrado es que los óvulos acumulan agregados, pero los acumulan dentro de los ELVAs, que en los óvulos inmaduros están inactivos. Y nosotros creemos que esto es una especie de forma de ahorro energético, porque, como el óvulo tiene que sobrevivir durante mucho tiempo, degradar constantemente, mantener constantemente activas estas estructuras, sería un gran coste energético», ha expresado el investigador.
«Entonces, el hecho de que estén inactivos permite secuestrar agregados de forma no tóxica y, al mismo tiempo, ahorrar energía, que al óvulo sirve luego para madurar», ha reiterado.
Aplicaciones en la infertilidad femenina
La mala calidad de los ovocitos es una de las principales causas de infertilidad femenina. En muchas ocasiones, la mala calidad se debe a defectos genéticos, asociados con la edad, pero existen otros factores desconocidos que alteran su viabilidad y supervivencia.
Por ello, esta investigación abre una vía futura de estudio para explorar si la degradación de proteínas y su mala regulación podría explicar el deterioro de la calidad ovocitaria relacionado con la edad.
Preguntado sobre este tema, Zaffagnini ha anunciado que están extendiendo esta investigación al envejecimiento reproductivo. «Es decir, todo esto está hecho en óvulos de ratones jóvenes, y ahora estamos empezando a mirar en óvulos de ratones ancianos que ya tienen envejecimiento reproductivo», ha señalado, para añadir que los ELVAs podrían tener “una regulación defectuosa”.
“También estamos empezando a colaborar con clínicas de fertilidad para mirar en óvulos humanos y ver si hay una regulación parecida”, ha finalizado Zaffagnini.
¿Posible aplicación en otro tipo de células?
Según Rocío Núñez Calonge, embrióloga, directora científica del Grupo Internacional UR y profesora en el Máster de Reproducción de la Universidad Complutense y Sociedad Española de Fertilidad, ha afirmado, al respecto de la investigación, que existen aún «numerosas dudas» que los mismos autores se plantean.
“¿Podrían existir compartimentos similares a los ELVA en otros tipos de células? Se ha postulado que podría ocurrir un mecanismo similar en las neuronas. Pero la forma en que estas células longevas, ovocitos y neuronas, transportan sus agregados de proteínas a compartimentos especializados y regulan su degradación, y si realmente esto sucede en las neuronas, siguen siendo futuras vías de investigación por explorar”, ha expresado la embrióloga.
A su juicio, la principal limitación es que se ha estudiado en ovocitos de ratón y hay que comprobar si realmente ocurre lo mismo en humanos.
«En el artículo, se compara con las neuronas porque comparten la similitud con los ovocitos de no dividirse y ser longevas, pero el objetivo del estudio y en lo que se centran es en los ovocitos y en su futura aplicación en los casos de infertilidad femenina. No entraría a hablar de Alzheimer. De hecho, en el artículo ni siquiera lo mencionan», ha apostillado.
Para acceder a IMMédico debe registrarse en el sitio.
Revise el texto completo del artículo en:



