Considerando que en el último mes se han detectado casos de fiebre de Oropouche en áreas que no hacen parte de la región amazónica en Brasil, además de la intensa circulación de dengue reportada por varios países y territoritos de la Región de las Américas, la Organización Panamericana de la Salud / Organización Mundial de la Salud (OPS/OMS) insta a los Estados Miembros a implementar las recomendaciones para el diagnóstico diferencial del virus Oropouche (OROV) y reforzar las medidas de vigilancia entomológica, control vectorial y de protección personal de la población a mayor riesgo.
Antecedentes
En la Región de las Américas, los brotes por el virus Oropouche (OROV) registrados en los últimos diez años han tenido lugar principalmente en la región amazónica. Históricamente, se han descrito numerosos brotes de enfermedad por OROV en comunidades rurales y urbanas de Brasil, Colombia, Ecuador, Guayana Francesa, Panamá, Perú y Trinidad y Tabago.
OROV se transmite al ser humano principalmente a través de la picadura del jején Culicoides paraensis que está presente en la Región de las Américas, pero también puede ser transmitido por el mosquito Culex quinquefasciatus.
Resumen de la situación
En lo que va del 2024, se han notificado 5.193 casos confirmados de Oropouche en cuatro países de la Región de las Américas: el Estado Plurinacional de Bolivia, Brasil, Colombia y Perú. Desde la última actualización epidemiológica de Oropouche de la Organización Panamericana de la Salud (OPS), Brasil y Bolivia han notificado casos en lugares donde no se habían registrado casos autóctonos previamente.
En Bolivia, durante el 2024, hasta la semana epidemiológica (SE) 18, se han notificado 1.856 casos sospechosos de Oropouche, de los cuales 313 han sido confirmados, por prueba de laboratorio RT-PCR en tiempo real. Se ha registrado la transmisión en tres departamentos y la confirmación por laboratorio en 16 municipios, siendo cuatro los nuevos municipios donde se han registrado casos confirmados desde la última actualización. El 66 % (n=235) de los casos se registra en el departamento de La Paz, seguido por Beni con el 21 % (n=68) y Pando con el 3 % (n=10). En cuanto a la distribución de los casos por sexo y grupo de edad, el 51% (n=157) corresponde a casos de sexo femenino y la mayor proporción en el grupo de edad de 30 a 39 años con el 21 % (n=66) de los casos.
En Brasil, entre la SE 1 y la SE 18 del 2024, se detectaron 4.583 casos confirmados de OROV. La mayoría de los casos han tenido como lugar probable de infección municipios de los estados del norte. La región amazónica, considerada endémica, concentra el 93 % de los casos registrados en el país: Amazonas (n=2.910), Rondônia (n=1.113), Acre (n=163), Pará (n=52), Roraima (n=7) y Amapá (n=1). Adicionalmente, se ha identificado la transmisión autóctona en tres estados no amazónicos donde no se habían registrado casos autóctonos previamente: Bahía (n=273), Espírito Santo (n=33) y Piauí (n=10). Así mismo, casos registrados en los estados de Rio de Janeiro (n=10), Santa Catarina (n=7) y Paraná (n=1), están siendo investigados para establecer el lugar probable de infección. En cuanto a la distribución de los casos por sexo y grupo de edad, el 52 % (n=2.396) corresponden a casos de sexo masculino y la mayor proporción de casos se registra en el grupo de edad de 20 a 29 años con el 21 % (n=977) de los casos (5, 10).
En Colombia, entre la SE 1 y la SE 18 del 2024, se detectaron 38 casos confirmados de Oropouche en tres departamentos del país: Amazonas (n=35), Caquetá (n=1), y Meta (n=1), adicionalmente se identificó un caso procedente de Tabatinga, Brasil. Los casos fueron identificados mediante una estrategia retrospectiva de búsqueda de casos por laboratorio implementada por el Instituto Nacional de Salud de Colombia (INS) a partir de la vigilancia de dengue. En cuanto a la distribución de los casos por sexo y grupo de edad, el 61 % (n=23) corresponden a casos de sexo masculino y la mayor proporción de casos se registra en el grupo de edad de 10 a 19 años con el 44 % (n=17) de los casos (11).
En Perú, entre la SE 1 y la SE 18 del 2024, se han registrado 259 casos confirmados de Oropouche en cuatro departamentos, siendo el mayor número de casos reportados a la fecha en este país. Los departamentos en donde se notificaron los casos confirmados son: Loreto (n=182), Madre de Dios (n=43), Ucayali (n=26) y Huánuco (n=8). En cuanto a la distribución de los casos por sexo y grupo de edad, el 51 % (n=131) corresponde al sexo masculino, la mayor proporción de casos se registra en el grupo de edad de 30 a 39 años con el 40 % (n=104) de los casos (12).
Diagnóstico clínico y manejo
Posterior a un periodo de incubación de 5 a 7 días los pacientes experimentan fiebre alta, cefalea con fotofobia, mialgias, artralgias y, en algunos casos, exantemas. En ciertos pacientes, los síntomas pueden incluir vómitos y hemorragias, manifestándose en forma de petequias, epistaxis y sangrado gingival. Generalmente, la infección se resuelve en un lapso de 2 a 3 semanas.
En situaciones excepcionales, el OROV puede provocar meningitis o encefalitis. En estos casos, los pacientes muestran síntomas y signos neurológicos como vértigo, letargia, nistagmos y rigidez de nuca. El virus puede ser detectado en el líquido cefalorraquídeo (LCR).
Durante la primera semana de la enfermedad, el principal diagnóstico diferencial es la infección por dengue. En la segunda semana de la enfermedad, el diagnóstico clínico diferencial debería considerar la posibilidad de meningitis y encefalitis.
Actualmente, no se disponen de vacunas ni medicamentos antivirales específicos para prevenir o tratar la infección por OROV. El enfoque del tratamiento es paliativo, centrado en aliviar el dolor, rehidratar al paciente y controlar cualquier vómito que pueda presentarse. En situaciones donde la enfermedad se manifieste de forma neuroinvasiva, será necesario el ingreso del paciente en unidades especializadas que permitan un monitoreo constante.
Diagnóstico y vigilancia por laboratorio
Las orientaciones sobre el diagnóstico y vigilancia por laboratorio de arbovirus emergentes, incluyendo OROV, se detallan en las “Directrices para la Detección y Vigilancia de Arbovirus Emergentes en el Contexto de la Circulación de Otros Arbovirus”.
Se sospecha que la circulación del virus incluye ciclos tanto epidémicos como selváticos. En el ciclo selvático, los primates, los perezosos y quizás las aves son los huéspedes vertebrados, aunque no se ha identificado un artrópodo vector definitivo. En el ciclo epidémico, el ser humano es el huésped amplificador y el OROV se transmite principalmente a través de la picadura del mosquito Culicoides paraensis. No se ha documentado la transmisión directa del virus de persona a persona.
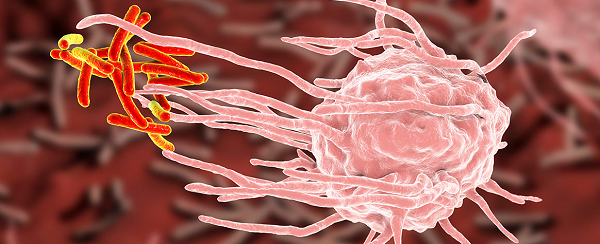
El virus OROV es un virus de ARN monocatenario que forma parte de la familia Peribunyaviridae; tiene un genoma segmentado con tres segmentos conocidos como S (del inglés small), M (del inglés medium) y L (del inglés large). Durante la fase aguda de la enfermedad, que dura habitualmente entre 2 y 7 días, es posible detectar el material genético del virus (ARN) por métodos moleculares (RT-PCR) en muestras de suero.
También es posible detectar el ARN en líquido cefalorraquídeo (LCR) en aquellos casos que se presentan con meningitis aséptica (complicación poco frecuente de la fiebre de Oropouche). La muestra de LCR solo debe ser tomada por indicación médica. La mayoría de los métodos moleculares se basan en la detección del segmento genético conservado S (15-17).
Prevención y control vectorial
La proximidad de criaderos de los vectores a los lugares de habitación humana es un factor de riesgo importante para la infección por OROV. Las medidas de control vectorial se enfocan en la reducción de las poblaciones de los vectores mediante la identificación y eliminación de los lugares de desarrollo y reposo de ellos.
Amplíe la información en: